محققان دانشگاه فلوریدا موفق به ایجاد روشی برای درمان نوع شایع نابینایی توسط ژن درمانی شدند. آنها با جایگزین کردن ژن معیوب توسط نسخه سالم آن که تولیدکننده پروتئین حساس به نور در چشم است به این مهم دست پیدا کردند.
این یافته در 23 ژانویه 2012 در ژورنال PNAS به چاپ رسیده است. با اینکه برای تکمیل این روش و کاربرد آن بر روی انسان، آزمایشات بیشتری مورد نیاز است اما دستآوردهای همین مرحله خود دارای پتانسیل خوبی به منظور تغییر زندگی بشر است.
دکتر ویلیام هاسویرس یکی از نویسندگان مقاله در مورد استفاده از این روش میگوید: " تصور کنید که شما به سختی میبینید و یا اصلاً قادر به دیدن نیستید و به وسیله استفاده از این روش این مشکلات برطرف شوند و شما قادر به خواندن، حرکت و یا حتی شاید رانندگی شوید در این هنگام زندگی شما به طور قابل ملاحظهای تغییر میکند." وی که استاد کرسی Rybaczki-Bullard چشم پزشکی دانشکده پزشکی فلوریدا و همچنین محقق برجسته در گروه ژنتیک مولکولی و میکروبیولوژی و موسسه ژنتیک این دانشگاه است افزود:"ترمیم قسمتی از ژن که نقص دارد یکی ازراههای غایی و نهایی درمان بیماری و بازگرداندن عملکرد معنیدار و قابل ملاحظه بینایی است."
دانشمندان با یک بیماری نقص ژنتیک به نام رتينيت پيگمانتوزا که یک بیماری وابسته به جنس است (رنگدانهاي شدن شبكيه چشم) روبه رو بودند که این بیماری از مادر به فرزند پسر به ارث میرسد و فرزندان دختر فقط ناقل آن هستند و همانند پسرها دچار نابینایی نمیشوند. حدود 100000 نفر در آمریکا مبتلا به این بیماری هستند که در آن ابتدا دید محیطی و دید در شب کم میشود و سرانجام منجر به حالتی به نام دید تونلی و در نهایت نابینایی را سبب میشود.
در بعضی موارد ازدست دادن بینایی به همراه ایجاد مناطقی سیاه رنگ بر روی شبکیه نارنجی رنگ چشم دیده میشود.
محققان این دانشگاه پیش از این در استفاده از ژن درمانی در مطالعات بالینی نوعی کوری مادرزادی به نام لبر پیشگام بودند. حدود 5 درصد از افراد مبتلا به بیماری رنگدانهاي شدن شبكيه چشم مبتلا به بیماری لبر، که برروی لایه داخلی چشم اثر دارد هستند.
به گفته پروفسور جان فلانری، استاد نوروبیولوژی در دانشگاه برکلی کالیفرنیا و متخصص در طراحی ویروسها برای انتقال ژن به عنوان حامل "این یک پیشرفت بسیار خوبی بود که نشان داد ژن درمانی بیخطر است و اثار آن برای سالها در انسان دوام دارد. امًا این مطالعه اخیر دارای پتانسیل بالاتری است زیرا درمان نوعی از بیماری را در بر دارد که بسیاری از مردم تحت تأثیر آن هستند."
بیماری رنگدانهای شدن شبکیه چشم در فرم وابسته به جنس (X.linked) که در این تحقیق مورد مطالعه قرار گرفته خیلی رایج است و به دلیل تحلیل و انحطاط سلولهای حساس به نور چشم موسوم به سلولهای دریافت کننده نور ایجاد میشود. این بیماری در اوایل زندگی آغاز میشود و با اینکه کودکان مبتلا در ابتدا دارای بینایی هستند ولی به تدریج آن را ازدست میدهند.
آلفرد لوین، استاد بخش ژنتیک مولکولی و میکروبیولوژی دانشکده پزشکی فلوریدا میگوید " این کودکان اغلب در دهه دوم زندگی خود که دورهای بسیار حیاتی است نابینا میشوند و این یک دلیل قانع کننده برای توسعه درمان آن است چراکه این بیماری سبب میشود تا مبتلایان نتوانند به طور کامل جهان پیرامون خود را تجربه کنند."
پژوهشگران دانشگاه فلوریدا و همکارانشان در دانشگاه پنسیلوانیا به وسیله همسانهسازی ژن مورد نظر در یک ویروس به عنوان ناقل برای حمل آن ژن به نقطه معینی از چشم و همچنین (همسانهسازی)کلون کردن ژنی که به عنوان یک کلید ژنتیک عمل میکند و فقط در زمانی که ژن مورد نظر در نقطه معین و دلخواه قرار گرفته باشد روشن میشود، توانستند پروتئینی که برای عملکرد سلولهای آسیب دیده چشم ضروری است را تولید کنند.
پس از موفقیت در تحقیقات آزمایشگاهی محققان با موفقیت در درمان حیواناتی که به طور طبیعی این بیماری را دارا بودند دامنه مطالعات خود را گسترش دادند. ژنهای منتقل شده تنها به نقطه تعریف شده برای آنها منتقل شدند و در سایر نقاط بدن مشاهده نشدند. این مطالعه برآورد خوبی از چگونگی کاربرد ژن درمانی در انسان را مشخص کرد.
به گفته فلانری عضو هیئت علمی بنیاد مبارزه با نابینایی و یکی از حامیان مالی این تحقیق " این نتایج دلگرم کننده است و رهایی از سلولهای دریافت کننده نور آسیب دیده، بسیار قانع کننده است؛ و از آنجایی که این مطالعه قدمی قبل از درمان افراد مبتلا به این بیماری است نشان دهنده انجام کاری بسیار حیاتی است"
پژوهشگران در پی این هستند که تحقیقات خود را در یک مقیاس وسیعتر انجام دهند و نسخهای از، ویروسی که برای انسان ضرر ندارد را ایجاد کنند. پس از بدست آمدن آن، یک کلاس دارویی از ویروس باید تهیه شود و قبل از استفاده در مطالعات بالینی مورد ارزیابی قرار بگیرد.
با استفاده از چنین پژوهشهایی دانشمندان در آینده میتوانند بینایی از دست رفته را بازگردانند.
ترجمه: فرنوش امینی
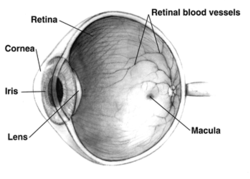

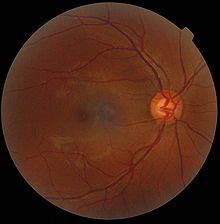
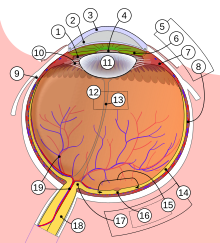




 این درمان حاصل بیش از 20 سال تلاش جین بنت، نسلشناس مولکولی دانشکده پزشکی دانشگاه پنسیلوانیا روی نابینایی ارثی در موشها و سگها است. خانم بنت میگوید، با مطالعه بیشتر، ظرف مدت 3 سال آینده میشود دارویی تولید کرد که بتواند توسط جراحان شبکیه برای درمان قطعی ال.سی.ای مورد استفاده قرار بگیرد. اما باز هم این پایان راه نخواهد بود. تنها سالانه 5 کودک در ایالات متحده متولد میشوند که مادرزاد مبتلا به نوعی ال.سی.ای هستند که خانم مورهاوس هم از آن رنج میبرد، اما میتوان با تمرکز روی درمان نقص در تکژنهای کمیاب و با استفاده از این تکنیک به راهی تازه برای درمان بیماریهای چشمی شایعتری دست یافت. دکتر بنت میگوید: «موفقیت ما نشان میدهد که این تکنیک پاسخگو است. ما امیدواریم این روش بتواند تکنیک نهایی برای درمان انواع بیماریهای منجر به نابینایی باشد. در خلال یکدهه، درمان ژنی خواهد توانست به بهبود بینایی در بیماران مبتلا به التهاب رنگدانهای شبکیه یا تخریب لکه زرد که هر دو ناشی از جهشهای دیگری در ژنها هستند نیز کمک کند».
این درمان حاصل بیش از 20 سال تلاش جین بنت، نسلشناس مولکولی دانشکده پزشکی دانشگاه پنسیلوانیا روی نابینایی ارثی در موشها و سگها است. خانم بنت میگوید، با مطالعه بیشتر، ظرف مدت 3 سال آینده میشود دارویی تولید کرد که بتواند توسط جراحان شبکیه برای درمان قطعی ال.سی.ای مورد استفاده قرار بگیرد. اما باز هم این پایان راه نخواهد بود. تنها سالانه 5 کودک در ایالات متحده متولد میشوند که مادرزاد مبتلا به نوعی ال.سی.ای هستند که خانم مورهاوس هم از آن رنج میبرد، اما میتوان با تمرکز روی درمان نقص در تکژنهای کمیاب و با استفاده از این تکنیک به راهی تازه برای درمان بیماریهای چشمی شایعتری دست یافت. دکتر بنت میگوید: «موفقیت ما نشان میدهد که این تکنیک پاسخگو است. ما امیدواریم این روش بتواند تکنیک نهایی برای درمان انواع بیماریهای منجر به نابینایی باشد. در خلال یکدهه، درمان ژنی خواهد توانست به بهبود بینایی در بیماران مبتلا به التهاب رنگدانهای شبکیه یا تخریب لکه زرد که هر دو ناشی از جهشهای دیگری در ژنها هستند نیز کمک کند».




 سلام من فرنوش امینی هستم و این پسرم ارشاد هست.
سلام من فرنوش امینی هستم و این پسرم ارشاد هست.